Le 17 déc. 2021
Recherche
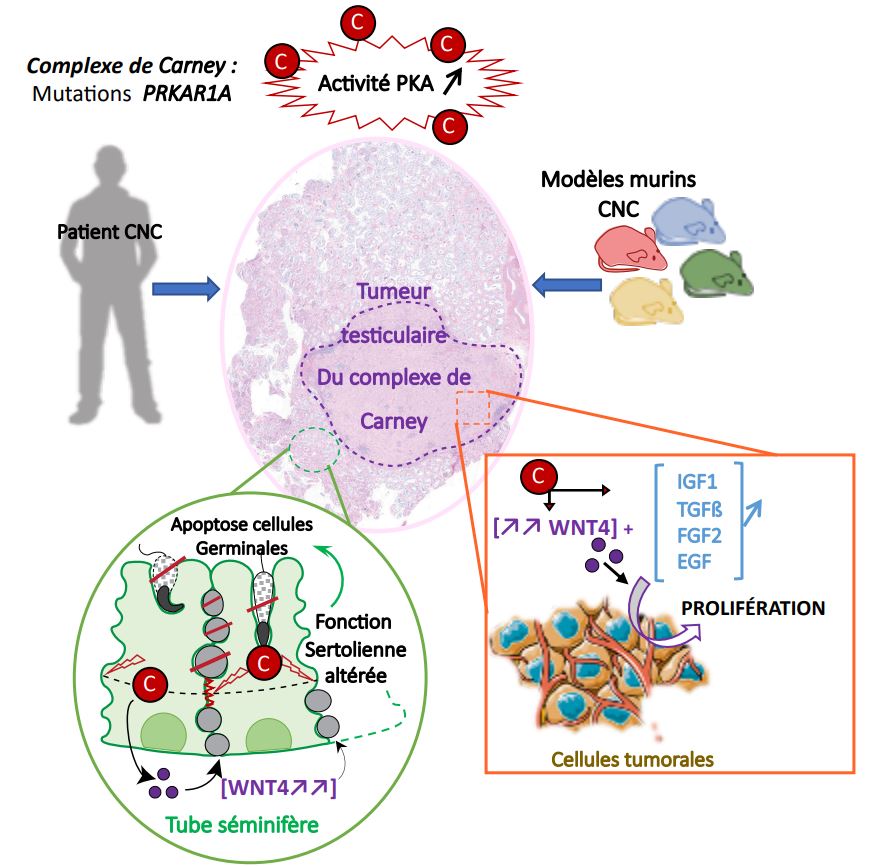
Tumorigénèse testiculaire du Complexe de Carney : Identification de nouveaux circuits de prolifération
Contact
Pr. A. Marie Lefran?ois-Martinez
Equipe ? Physiopathologie moléculaire de la surrénale & des tissus endocrines ?
Institut GReD CNRS 6293 INSERM1103 Université Clermont Auvergne
a-marie.lefrancois-martinez@uca.fr
04 73 40 77 59